基本信息
- 中文名称
- 乐伐替尼
- 英文名称
- Lenvatinib
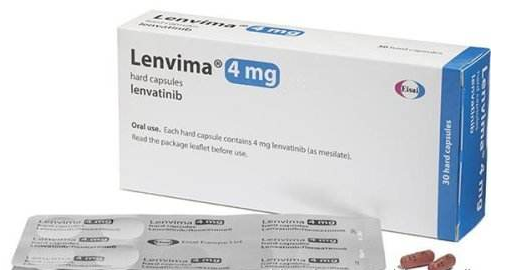
- 商品名
- Lenvima
适应症
乐伐替尼适应症1:LENVIMA是一种激酶抑制剂适用为有局部地复发或转移,进展性,放射性碘-难治性分化型甲状腺癌患者的治疗(1)。分化型甲状腺癌(DTC):患者的局部复发或转移性,进取,放射性碘难治性DTC单剂。(2015年上市在美国、欧盟及日本上市用于治疗分化型甲状腺癌)
乐伐替尼适应症2:肾细胞癌(RCC):与依维莫司联合,对于晚期RCC下面有一个事先的抗血管生成治疗。(2016年5月,乐伐替尼在美国被FDA批准与依维莫司联合用药,治疗既往接受过血管内皮生长因子靶向疗法的晚期肾细胞癌患者。)
乐伐替尼适应症3:肝细胞癌。
用法用量
推荐剂量1:24 mg口服,每天一次(2.1)。
推荐剂量2:在有严重肾或肝受损患者,剂量是14 mg每天一次(2.1)。
推荐剂量3:肾细胞癌(RCC):18毫克LENVIMA+5毫克依维莫司,口服,每日一次。
警告
⑴ 高血压:用LENVIMA治疗前控制血压。对尽管优化高血压治疗的3级高血压不给LENVIMA。对危及生命高血压终止药物(5.1)。
⑵ 心力衰竭:监视心脏代偿失调的临床症状和体征。对3级不给LENVIMA心功能不全。对4级心功能不全终止药物(5.2)。
⑶ 动脉血栓栓塞事件:一次动脉血栓栓塞事件后终止LENVIMA(5.3)。
⑷ 肝毒性: LENVIMA开始前和治疗自始至终定期地监视肝功能检验. 对3级或更大肝受损不给LENVIMA。对肝衰竭终止治疗(5.4)。
⑸ 蛋白尿:用LENVIMA开始治疗前,和自始至终定期地,监视蛋白尿。对24小时尿蛋白≥2 克不给LENVIMA。对肾病综合征终止用药(5.5)。
⑹ 肾衰竭和肾受损: 对3或4级肾衰竭/受损不给LENVIMA (5.6)。
⑺ 胃肠道穿孔和瘘管形成:发生胃肠道穿孔或危及生命瘘管患者中终止LENVIMA (5.7)。
⑻ QT间期延长:在所有患者中监视和纠正电解质异常。对发生3级或更大QT间期延长不给LENVIMA (5.8)。
⑼ 低钙血症:监视血钙水平至少每月和需要时给予替代钙(5.9)。
⑽ 可逆性后部白质脑病综合征(RPLS): 对RPLS不给LENVIMA直至完全解决(5.10)。
⑾ 出血事件:对3级出血不给LENVIMA。对4级出血终止治疗(5.11)。
⑿ 甲状腺刺激激素抑制的受损:每月监视TSH水平和有DTC患者需要时调整甲状腺取代药物 (5.12)。
⒀ 胚胎胎儿毒性:可能致胎儿危害。忠告对胎儿潜在风险和使用有效避孕(5.13,8.1,8.3)。
不良反应
对LENVIMA最常见不良反应(发生率大于或等于30%)是高血压,疲乏,腹泻,关节痛/肌肉痛,食欲减退,体重减轻,恶心,口炎,头痛,呕吐,蛋白尿,掌,跖红肿综合征,腹痛,和发音困难。
药物相互作用
当LENVIMA与CYP3A,P糖蛋白(P-gp),和乳癌耐药蛋白(BCRP)抑制剂和CYP3A和P-gp诱导剂共同给药是无剂量调整的建议[见临床药理学(12.3)]。
特定人群使用
8.1 妊娠
风险总结
根据其作用机制和来自动物生殖研究数据,当给予妊娠妇女时LENVIMA可能致胎儿危害[见临床药理学(12.1)]。在动物生殖研究,在器官形成期口服给予大鼠和兔lenvatinib在推荐人用剂量导致胚胎毒性,胎儿毒性,和致畸胎性[见数据]。药物-关联毒性没有可得到的人类数据信息。忠告妊娠妇女对胎儿潜在风险。
不知道对适用人群重大出生缺陷和流产对背景风险;但是,在美国一般人群重大出生缺陷背景风险为2-4%和流产是临床上识别的妊娠对15-20%。
数据
动物数据
在一项胚胎胎儿发育研究,在器官形成期每天口服给予lenvatinib甲磺酸盐在剂量大于或等于0.3 mg/kg[根据体表面积(BSA)为推荐人用剂量约0.14倍]至妊娠大鼠导致均数胎儿体重剂量-相关减低,延迟胎儿骨化,和胎儿外(胃壁水肿和尾部异常),内脏,和骨骼异常剂量-相关增加。在1.0 mg/kg/day(根据BSA推荐人用剂量约0.5倍)观察到植入后丢失大于80%。
妊娠兔器官形成期时每天口服给予lenvatinib甲磺酸盐导致胎儿外(短尾),内脏(食道后锁骨下动脉),和骨骼异常在剂量大于或等于0.03 mg/kg(根据体表面积人用剂量24 mg的约0.03倍)。在0.03 mg/kg剂量,还观察到增加植入后丢失,包括1只胎兔死亡。Lenvatinib在兔中有堕胎作用,在0.5 mg/kg/day剂量水平(根据BSA为推荐人临床剂量24 mg约0.5倍)导致三分之一被处理兔晚期流产。
8.2 哺乳
风险总结
不知道LENVIMA是否存在于人乳汁。但是,lenvatinib及其代谢物被排泄在大鼠乳汁中浓度较高于母鼠血浆[见数据]。因为哺乳婴儿来自LENVIMA对严重不良反应潜能,忠告妇女用LENVIMA治疗期间终止哺乳喂养。
数据
动物数据
哺乳Sprague Dawley大鼠给予放射性标记lenvatinib后,在乳汁中lenvatinib-相关放射性与母鼠血浆比较约较高2倍(根据AUC)。
8.3 有生殖潜能的女性和男性
避孕
根据其作用机制,当给予妊娠妇女LENVIMA可能致胎儿危害[见特殊人群中使用(8.1)]。忠告 有生殖潜能女性在用LENVIMA治疗期间和完成治疗后至少2周使用有效避孕。
不孕不育
女性
在有生殖潜能女性中LENVIMA可能导致生育力减低[见非临床毒理学(13.1)]。
男性
LENVIMA可能导致男性生殖组织损伤导致未知时间的生育力减低[见非临床毒理学(13.1)]。
8.4 儿童使用
未曾确定LENVIMA在儿童患者中安全性和有效性。
幼年动物数据
幼年大鼠在产后第21天开始每天口服给予lenvatinib甲磺酸盐共8周(约等于一例人儿童年龄2岁)导致生长迟缓(减低体重增量,减低食耗量,和减低股骨胫骨宽度和/或长度)和在剂量大于或等于2 mg/kg(按AUC在推荐人用剂量临床暴露约1.2至5倍)继发延迟身体发育和器官未成熟。恢复的4周后股骨和胫骨长度持续减低。一般说来,在幼年和成年大鼠至lenvatinib的毒理学图形相似,虽然在幼年大鼠中毒性包括在所有剂量水平断牙和在10 mg/kg/day剂量水平时在早期治疗时间-点发生死亡率(主要十二指肠病变贡献)。
8.5 老年人使用
在研究1中261例接受LENVIMA患者中,118(45.2%)为大于或等于65岁和29(11.1%)为大于或等于75岁,这些受试者和较年轻受试者间未观察到安全性或有效性总体差别。
8.6 肾受损
在轻度或中度肾受损患者建议无剂量调整。在有严重肾受损患者中,推荐剂量是14 mg服用每天一次。没有研究有肾病终末期患者[见剂量和给药方法(2.1),警告和注意事项(5.6),临床药理学(12.3)]。
8.7 肝受损
有轻度或中度肝受损患者建议无剂量调整。有严重肝受损患者,推荐剂量是14 mg服用每天一次[见剂量和给药方法(2.1),临床药理学(12.3)]。
康安途医疗旅游 时间:2018-09-15 所属标签:乐伐替尼,乐卫玛,仑伐替尼
- 词条统计
-
- 浏览次数: 25472次
- 最近更新: 2018-08-29
- 创建者: 新垣结衣